Im letzten TGD-Rundschreiben wurde darauf hingewiesen, dass Sonderimporte am Abgabebeleg entsprechend dokumentiert werden müssen. Lt. TGD müssen bei Sonderimporten folgende Informationen am Abgabebeleg zusätzlich folgende Informationen gedruckt werden.
- Der Vermerk „Sonderimport“ (ANIMALoffice erkennt an diesem Wort, dass die Infos auch bei Anwendung gedruckt werden müssen).
- Zulassungsnummer des Arzneimittels lt. Verpackung. Dabei handelt es sich um die Zulassungsnummer des Landes aus dem das Arzneimittel importiert wurde.
- Wartezeiten wie auf der Arzneimittelpackung angegeben od. Kaskadenregelung.
Nachdem bei uns mehrere Kollegen um einen entsprechenden Lösungsvorschlag angefragt haben, dürfen wir nachstehend die folgende Empfehlung geben:
ANIMALoffice Artikelstamm
Im ANIMALoffice Artikelstamm können nur Zulassungsnummern erfasst werden, welche in der AGES-Datenbank existieren d.h. auch in Österreich zugelassen sind. Bei Sonderimporten ist daher keine Eingabe im Feld „Zulassungsnummer“ möglich. Aus diesem Grund empfehlen wir den folgenden Workarround:
- Erstellen Sie für das Arzneimittel, wie gewohnt, einen neuen Stammsatz im Artikelstamm.
- Tragen Sie die Wartezeiten manuell ein.
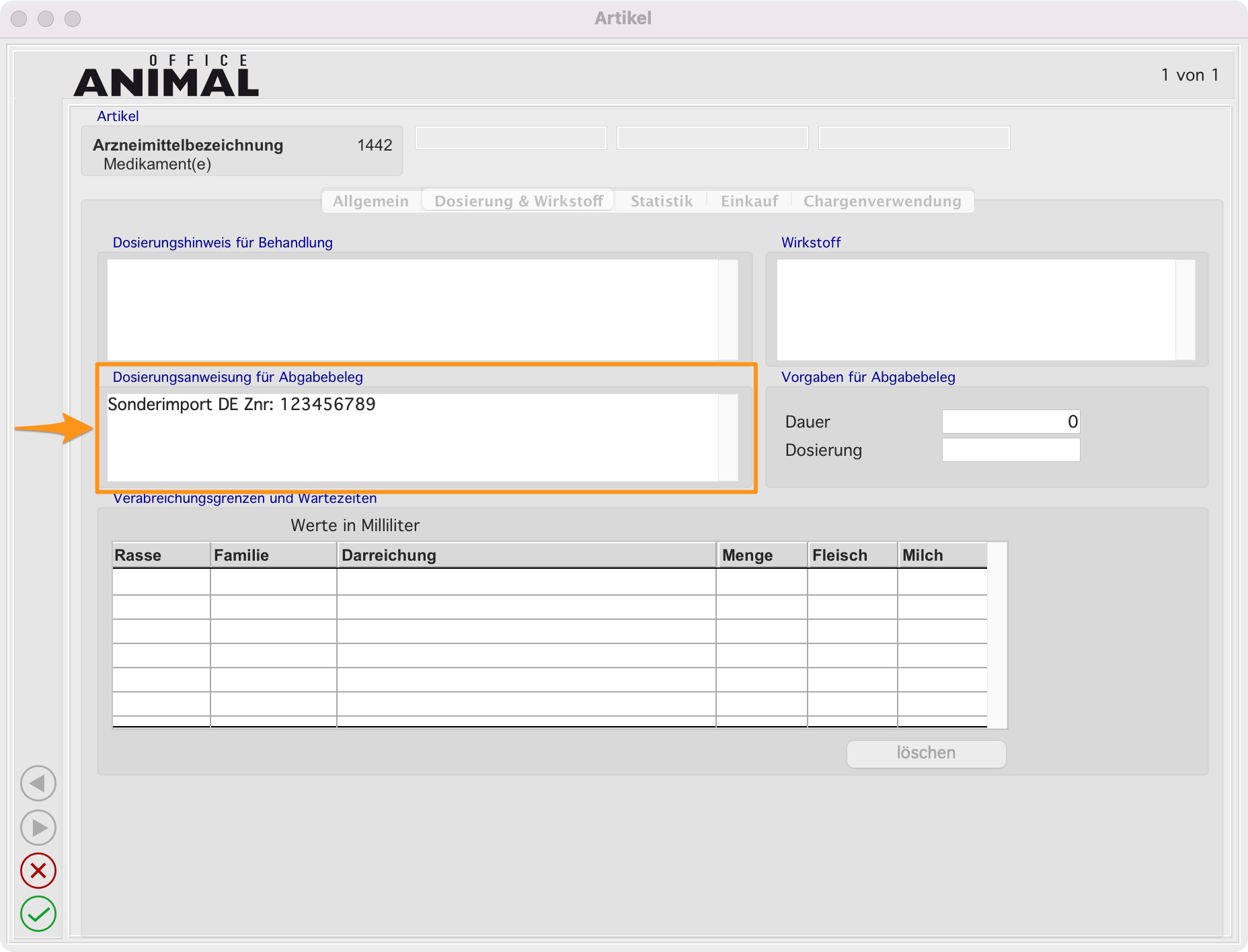
- Bei den Bestandsangaben wechseln Sie zum TAB Dosierung & Wirkstoff.
-
Schreiben Sie im Feld Dosierungsanweisung für Abgabebeleg die folgenden Angaben:
- „Sonderimport“ - fixer Text.
- „DE“ - Länderkennzeichen Importland.
- „Znr.: 1234567“ - Zulassungsnummer Verpackung.
Der fixe Text “Sonderimport“ ist wichtig, da ANIMALoffice beim Druck des Abgabebelegs, in diesem Fall den Inhalt des Feldes auch bei einer Anwendung des Arzneimittels berücksichtigt.
ANIMALoffice Abgabebeleg
Diese Informationen werden bei der Verwendung des Arzneimittels im Rahmen einer Behandlung in der Folge automatisch am Abgabebeleg gedruckt.
Beispiel:

Bei Bedarf können Sie in diesem Feld auch weitere Infos erfassen. Auf diese Weise dokumentieren Sie auch Arzneimittel aus Sonderimporten immer korrekt.